V mojich príspevkoch píšem najmä o jadrovej energii, aj o subjadrových časticiach.
Ale existuje oblasť – dala by sa stále povedať dokonca „mysteriózna“, ktorá sa pohybuje na rozhraní fyziky, chémie a biológie súčasne. Rozmerovo sa zvyčajne pohybuje o trošku vyššie ako je jadro atómu (trochu vo väčších rozmeroch, aj keď vlastne stále veľmi maličkých) – na molekulovej úrovni a teda by sa nám malo na prvý pohľad zdať že tam už všetko vieme, ale opak je pravdou.
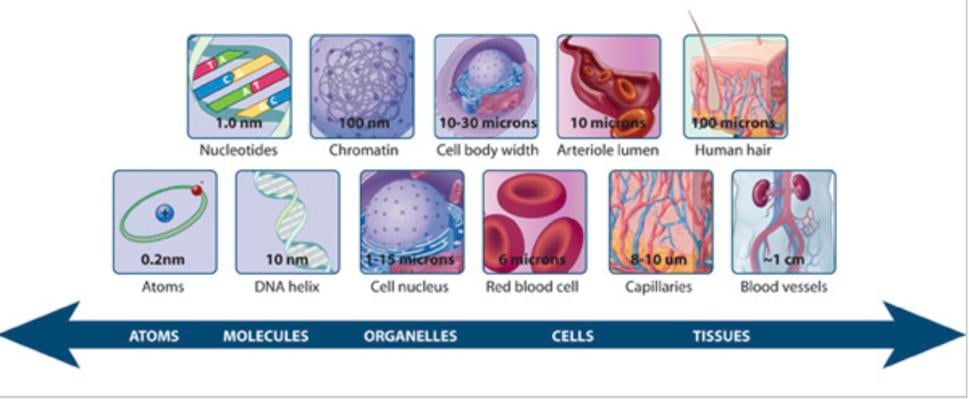
Aj tu sa však tieto procesy dotýkajú na úrovni protónov a elektrónov.
Je tam toho ešte až príliš mnoho neznámeho a paradoxne to súvisí dokonca bezprostredne s absolútne fundamentálnymi otázkami nášho života.
Skúsme sa na to spoločne pozrieť....
Odkiaľ pochádza energia, ktorá umožňuje náš život?
Je to energia je zachytená v chemických väzbách molekúl živín.
Ľudia získavajú energiu z troch tried molekúl paliva: uhľohydrátov, lipidov a bielkovín.
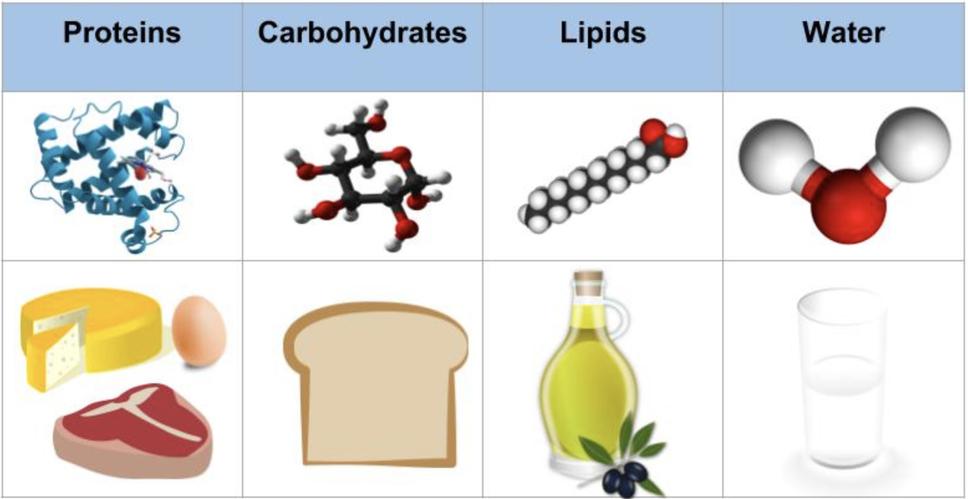
Potenciálna chemická energia týchto molekúl sa transformuje do iných foriem, ako sú tepelné, kinetické a iné chemické formy.
Ale ako to funguje a je to potom využiteľné pre bunkové funkcie a bio syntetické procesy.
Živiny ľudského metabolizmu
Sacharidy, lipidy a bielkoviny sú hlavnými zložkami potravín a slúžia ako molekuly paliva pre ľudské telo.
Trávenie (rozklad na menšie kúsky) týchto živín v zažívacom trakte a následná absorpcia (vstup do krvného obehu) konečných produktov trávenia umožňuje tkanivám a bunkám premeniť potenciálnu chemickú energiu potravy na užitočnú prácu.
Hlavnými absorbovanými konečnými produktmi trávenia potravy sú monosacharidy, najmä glukóza (zo sacharidov); monoacylglycerol a mastné kyseliny s dlhým reťazcom (z lipidov); a malé peptidy a aminokyseliny (z bielkovín). Tieto, keď sa dostanú do krvného obehu, tak ich rôzne bunky môžu (tieto živiny) metabolizovať.
Už dlho sa vie, že práve tieto tri triedy molekúl sú palivovými zdrojmi pre ľudský metabolizmus, napriek tomu je bežnou mylnou predstavou (dokonca aj medzi ľuďmi s vysokoškolským vzdelaním), že ľudské bunky využívajú ako zdroj energie iba glukózu.
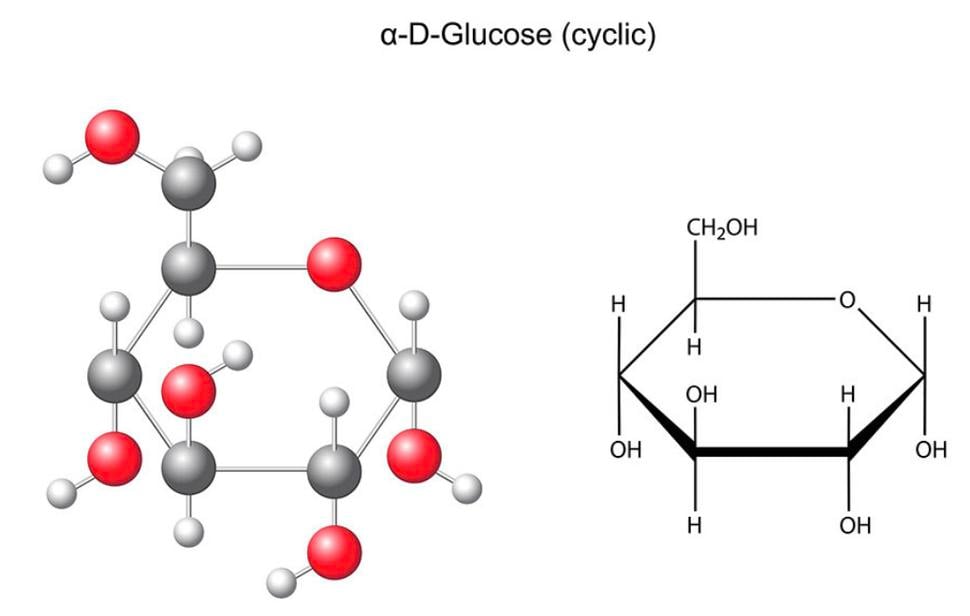
Možno to vyplýva zo spôsobu, akým väčšina učebníc vysvetľuje energetický metabolizmus, keď zdôrazňujú glykolýzu (metabolickú dráhu degradácie glukózy) a napríklad vynechajú oxidáciu mastných kyselín alebo aminokyselín. Ide o to, že ako tri živiny (sacharidy, bielkoviny a lipidy) metabolizujú v ľudských bunkách spôsobom, lebo inak to bude neucelený - príliš zjednodušený pohľad na metabolizmus.
Trochu histórie okolo výskumov energetického metabolizmu.
Už počas osemnásteho storočia zohrali počiatočné štúdie, ktoré vypracovali Joseph Black, Joseph Priestley, Carl Wilhelm Scheele a Antoine Lavoisier, osobitnú úlohu pri identifikácii dvoch plynov, a to kyslíka a oxidu uhličitého, ktoré sú kľúčové pre energetický metabolizmus.

Antoine Lavoisier, francúzsky šľachtic, ktorému sa hovorí „otec modernej chémie“, vtedy charakterizoval zloženie vzduchu, ktorý dýchame, a tiež aj uskutočnil prvé experimenty ohľadom energie v ľudskom organizme.
Jedna z hlavných Lavoisierových otázok v tejto dobe bola: „Ako súvisí úloha kyslíka pri spaľovaní s procesom dýchania v živých organizmoch?“
Pomocou kalorimetra na kvantitatívne merania s morčatami a neskôr aj sám so sebou a so svojím asistentom ukázal, že dýchanie je vlastne pomalá forma spaľovania. Na základe tohto konceptu, že kyslík vlastne spaľuje uhlík v potravinách, Lavoisier ukázal, že vydychovaný vzduch obsahuje oxid uhličitý, ktorý vznikol reakciou medzi kyslíkom (prítomným vo vzduchu) a organickými molekulami vo vnútri organizmu.
Lavoisier tiež zistil, že telo počas dýchania neustále produkuje teplo. V polovici devätnásteho storočia, vykonal štúdie na zvieratách zase Justus Liebig a zistil, že bielkoviny, sacharidy a tuky sa v tele oxidujú. No a napokon, priekopnícky príspevok k metabolizmu a výžive pochádza zo štúdií Liebigovho chránenca Carla von Voita a jeho talentovaného študenta Maxa Rubnera. Voit preukázal, že spotreba kyslíka je výsledkom bunkového metabolizmu, zatiaľ čo Rubner meral hlavnú energetickú hodnotu určitých potravín, aby vypočítal kalorické hodnoty (ktoré sa mimochodom používajú dodnes).
Napríklad sacharidy a bielkoviny produkujú približne 4 kcal/g energie, zatiaľ čo lipidy môžu generovať až 9 kcal/g.

Rubnerove pozorovania dokázali, že pre odpočívajúceho živočícha bola jeho produkcia tepla ekvivalentná jeho eliminácii tepla, čo potvrdilo, že zákon zachovania energie, vyplývajúci z Lavoisierových skorších experimentov, bol aplikovateľný aj na živé organizmy.
Takže to, čo umožňuje (aj náš) život, je transformácia potenciálnej chemickej energie molekúl paliva prostredníctvom série reakcií v bunke, ktoré umožňuje kyslík, na iné formy energie – a to chemickej, pohybovej, kinetickej a tepelnej.
Dá sa povedať že univerzálnym platidlom všeobecne v prírode a v našom živote je vlastne energia!

Na to živé bunky zostali nažive, rástli a rozmnožovali sa nepotrebujú žiadne veci či módne výmysly, ale nevyhnutne potrebujú energiu!
A tento všeobecný proces, ktorým získavajú a využívajú energiu potrebnú na to, aby prežili je tzv. „Energetický metabolizmus“.
A ako to funguje?
Výroba a úspora energie v ľudskom tele je zabezpečovaná uvoľňovaním energie pri rozbíjaní (uvoľňovaní) chemických väzieb molekúl živín zachytených bunkami na iné použitie. Je to v spojení medzi oxidáciou živín a syntézou vysoko energetických zlúčenín, najmä tzn. „ATP“, ktorý funguje ako hlavný chemický nosič energie (teda to univerzálne platidlo) vo všetkých našich bunkách.
Mechanizmy syntézy ATP
Čo je to ATP?
„ATP“ je skratka pre „Adenozíntrifosfát“, čo je chemická zlúčenina patriaca medzi nukleotidy; chemicky ide o trifosforylovaný adenozín s dvomi makroergickými väzbami. ATP slúži predovšetkým ako prenášač fosfátu v rámci energetického metabolizmu bunky a univerzálny zdroj energie všetkých živých organizmov.
Existujú dva mechanizmy syntézy ATP:
1. oxidačná fosforylácia, proces, ktorým sa ATP syntetizuje z ADP a anorganického fosfátu (Pi), ktorý prebieha v mitochondriách; a
2. fosforylácia na úrovni substrátu, pri ktorej sa ATP syntetizuje prenosom vysoko energetických fosforylových skupín z vysoko energetických zlúčenín na ADP.
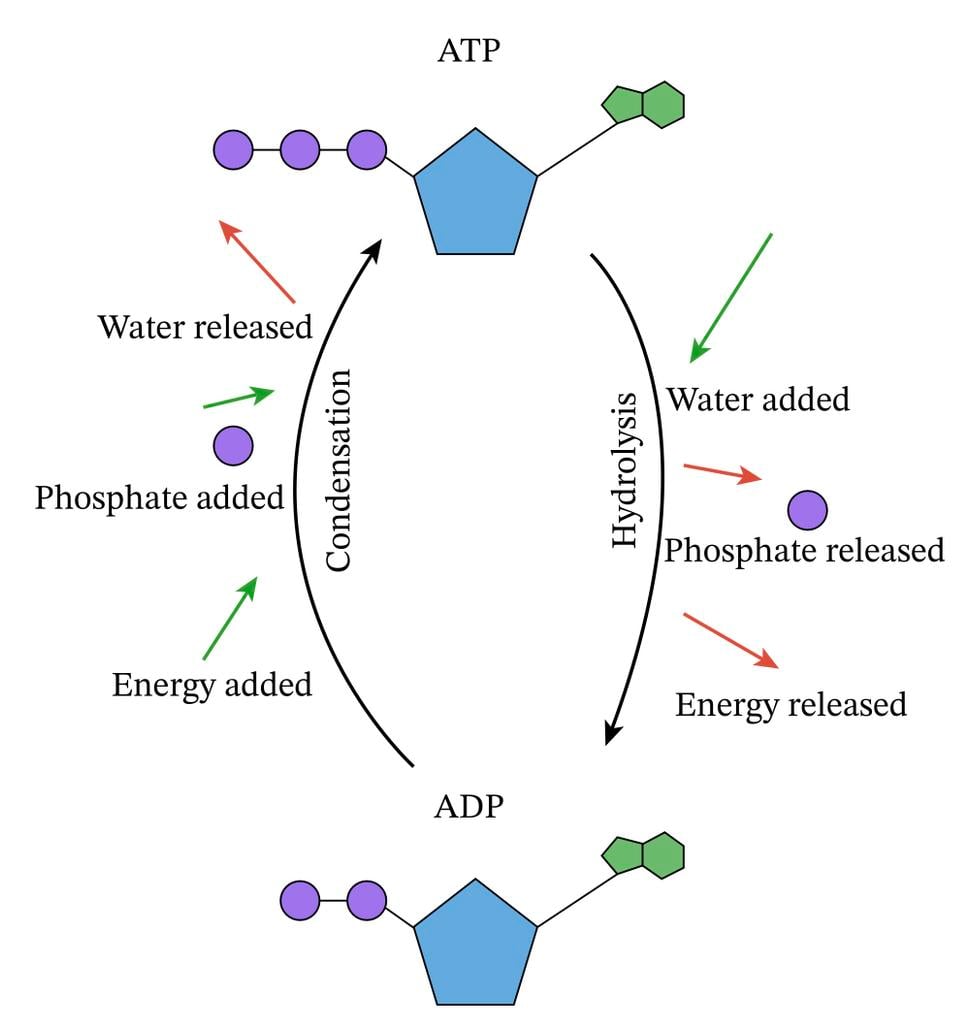
ATP predstavuje primárny zdroj energie pre bunku. Energia sa uvoľňuje prihydrolytickom štiepení molekuly kyseliny trihydrogenfosforečnej z molekuly ATP, pričom vzniká adenozíndiofosfát, ktorý má zase skratku „ADP“. Ten sa vyskytuje v mitochondriách počas cyklu trikarboxylových kyselín (TCA) a v cytoplazme počas glykolýzy.
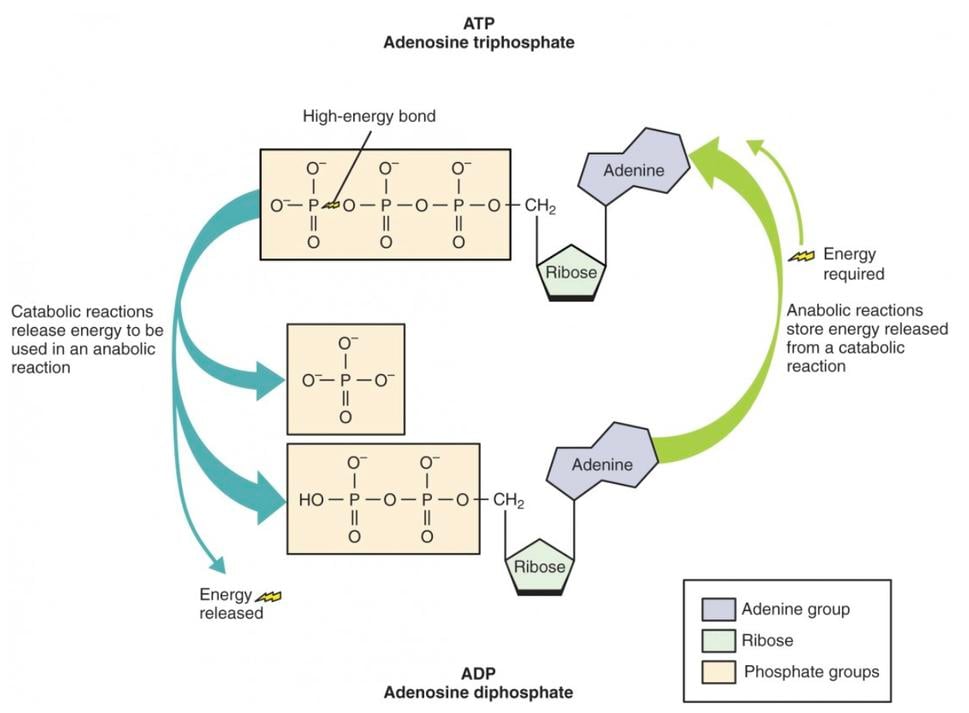
Hlavný mechanizmus syntézy ATP vo väčšine ľudských buniek ide cez oxidačnú fosforyláciu. A existuje aj niekoľko iných metabolických ciest (dráh), v ktorých sú tri triedy molekúl živín degradované.
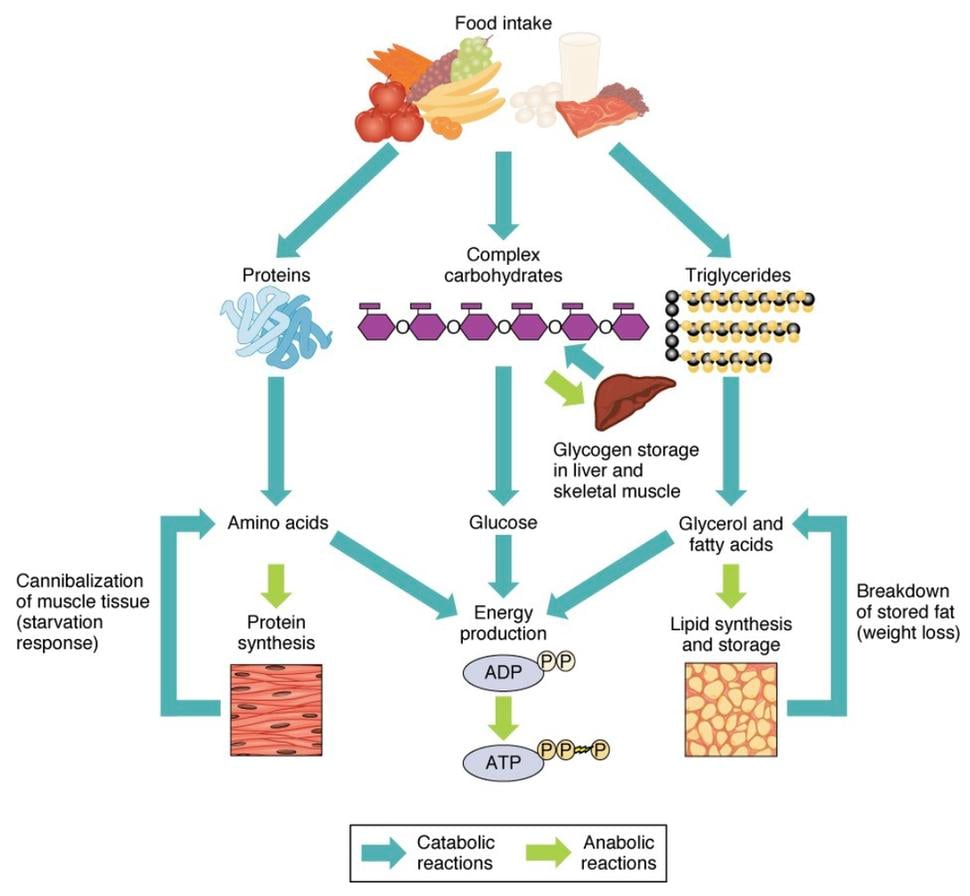
Metabolické reakcie sú procesy prenášajúce energiu, pri ktorých sú oxidačno-redukčné reakcie životne dôležité pre syntézu ATP. V týchto reakciách sa elektróny odstránené oxidáciou molekúl paliva prenesú na dva hlavné koenzýmy prenášajúce elektróny, nikotínamid adenín dinukleotid (NAD+) a flavín adenín dinukleotid (FAD), ktoré sa premieňajú na svoje redukované formy NADH a FADH2.
Oxidačná fosforylácia závisí od transportu elektrónov z NADH alebo FADH2 do O2, pričom vzniká H2O.
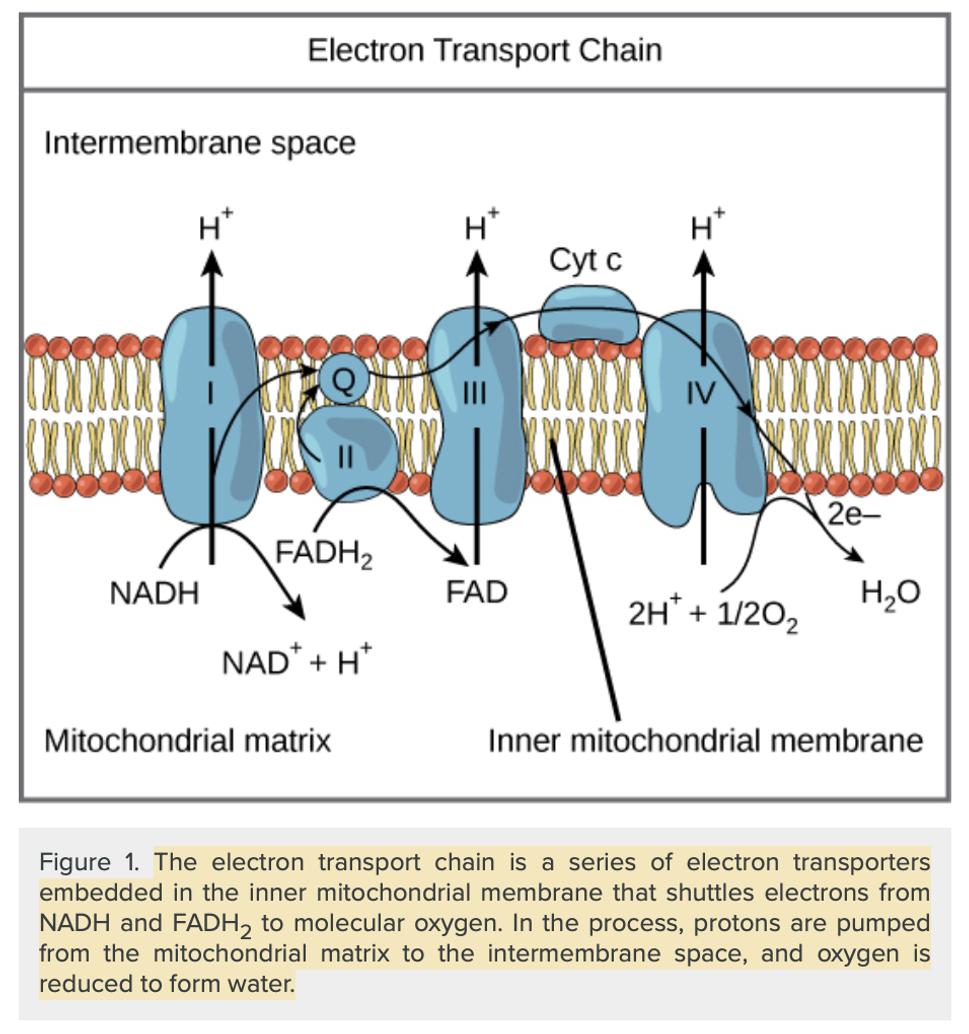
Elektróny sú „transportované“ cez množstvo proteínových komplexov umiestnených vo vnútornej mitochondriálnej membráne, ktorá obsahuje pripojené chemické skupiny (flavíny, skupiny železa a síry, hém a ióny medi) schopné prijať alebo darovať jeden alebo viac elektrónov. Tieto proteínové komplexy, známe ako systém prenosu elektrónov (ETS), umožňujú distribúciu voľnej energie medzi redukované koenzýmy a O2 a efektívnejšie šetrenie energie.
Elektróny sa prenášajú z NADH do O2 prostredníctvom troch proteínových komplexov:
- NADH dehydrogenáza,
- cytochróm reduktáza a
- cytochróm oxidáza.
Transport elektrónov medzi komplexmi prebieha prostredníctvom iných mobilných nosičov elektrónov, ubichinónu a cytochrómu c.
FAD je spojený s enzýmom sukcinátdehydrogenázou cyklu TCA a ďalším enzýmom, acyl-CoA dehydrogenázou z dráhy oxidácie mastných kyselín.
Počas reakcií katalyzovaných týmito enzýmami sa FAD redukuje na FADH2, ktorého elektróny sa potom prenesú na O2 prostredníctvom cytochrómreduktázy a cytochrómoxidázy.
Prenos elektrónov cez zložky ETS je spojený s pumpovaním protónov (H+) z mitochondriálnej matrice do medzimembránového priestoru mitochondrií.
Tieto pozorovania viedli Petra Mitchella v roku 1961 k navrhnutiu jeho revolučnej chemiosmotickej hypotézy.
V tejto hypotéze Mitchell navrhol, že pumpovanie H+ generuje to, čo nazval „protónová hybná sila“, kombináciu pH gradientu cez vnútornú mitochondriálnu membránu a transmembránový elektrický potenciál, ktorý poháňa syntézu ATP z ADP a Pi.
ATP je syntetizovaný komplexom ATP syntázy, cez ktorý sa H+ protóny vracajú do mitchondriálnej matrice.
Katalytický mechanizmus ATP syntázy prvýkrát opísal Paul Boyer a ukázal, že vstup energie z H+ gradientu sa použil na uvoľnenie ATP z katalytického miesta a že tri aktívne miesta enzýmu spolupracovali takým spôsobom, že ATP z jedného miesta nemohol byť uvoľnený, pokiaľ ADP a Pi neboli dostupné na naviazanie na iné miesto.
Oxidácia sacharidov, bielkovín a tukov sa zbieha v cykle trikarboxylových kyselín
Vzájomná premena energie medzi redukovanými koenzýmami a O2 riadi syntézu ATP, ale ako (a kde) sa znižuje NADH a FADH2?
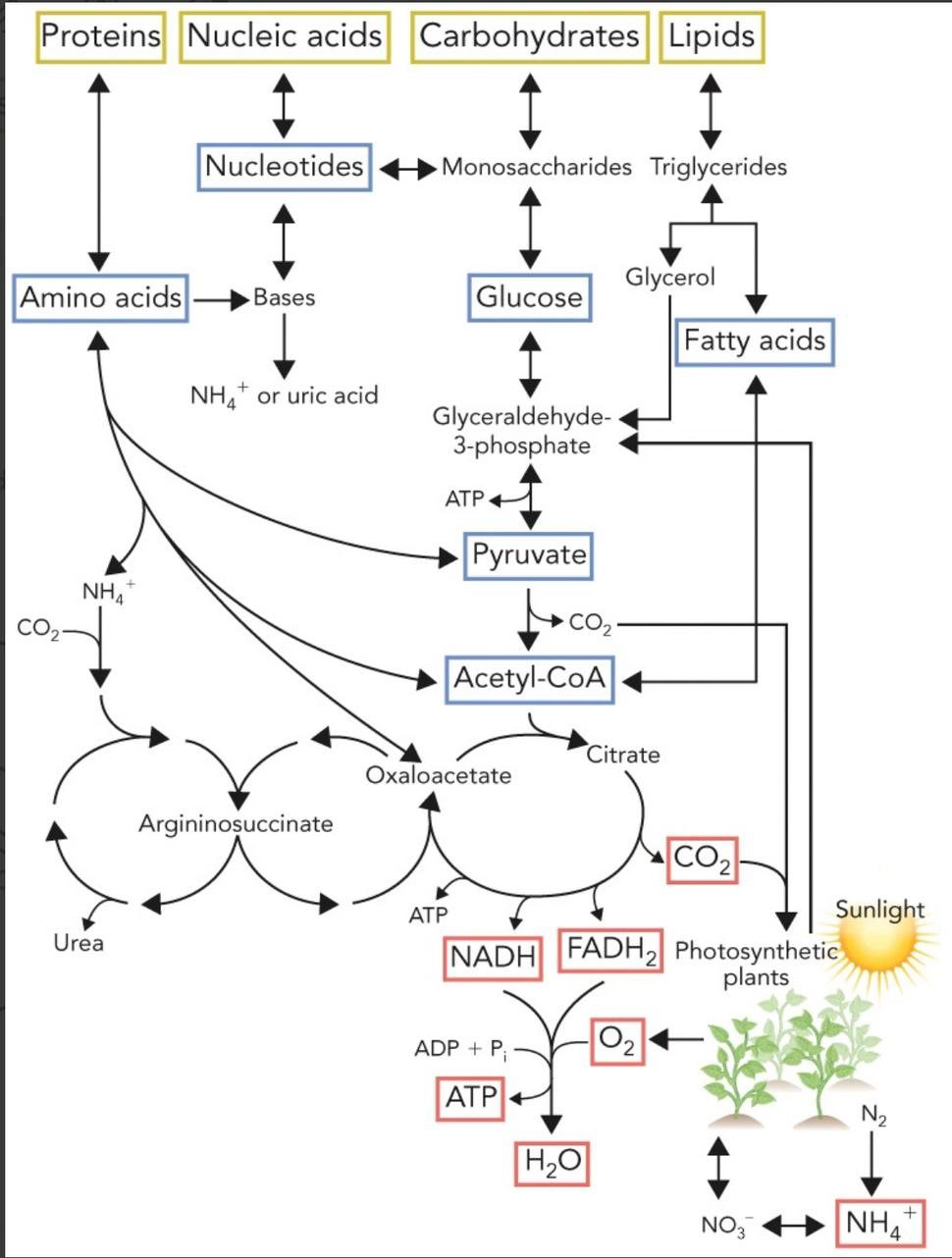
Pri aeróbnom dýchaní alebo aerobióze sa všetky produkty degradácie živín zbiehajú do centrálnej metabolickej dráhy, cyklu TCA.
V tejto dráhe sa acetylová skupina acetyl-CoA, ktorá je výsledkom katabolizmu glukózy, mastných kyselín a niektorých aminokyselín, úplne oxiduje na CO2 so súčasnou redukciou koenzýmov prenášajúcich elektróny (NADH a FADH2).
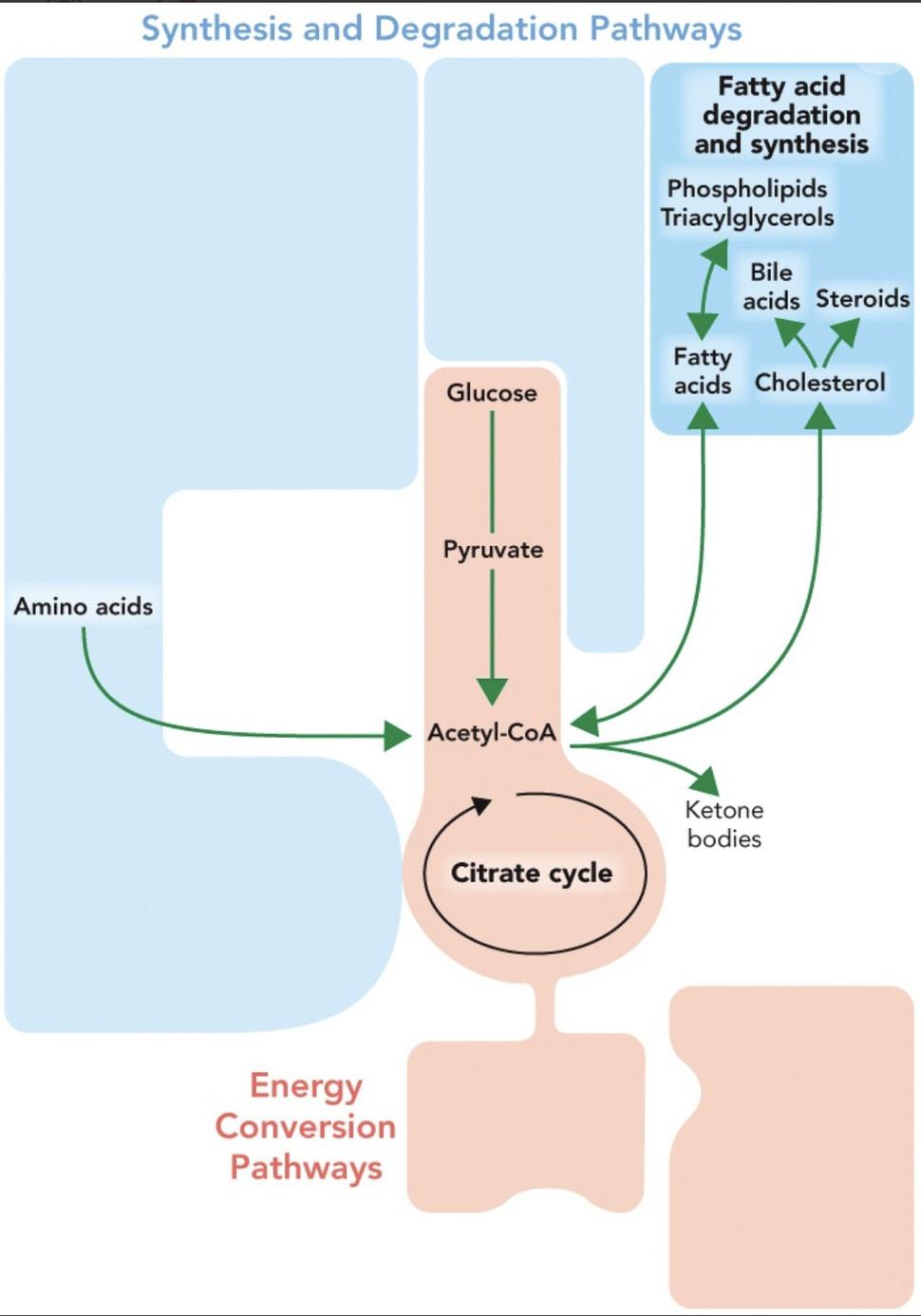
Cyklus pozostávajúci z ôsmich reakcií začína kondenzáciou acetyl-CoA a oxaloacetátu za vzniku citrátu.
Nasledujúcich sedem reakcií regeneruje oxalacetát a zahŕňa štyri oxidačné reakcie, pri ktorých sa energia šetrí redukciou koenzýmov NAD+ a FAD na NADH a FADH2, ktorých elektróny sa potom prenesú na O2 prostredníctvom ETS.
Okrem toho sa priamo vytvára molekula GTP alebo ATP ako príklad fosforylácie na úrovni substrátu. V tomto prípade je hydrolýza tioesterovej väzby sukcinyl-CoA so sprievodnou enzýmovou fosforyláciou spojená s prenosom fosfátovej skupiny viazanej na enzým na GDP alebo ADP.
Dôležité je, že hoci sa O2 priamo nezúčastňuje tejto dráhy, cyklus TCA funguje iba v aeróbnych podmienkach, pretože oxidované NAD+ a FAD sa regenerujú iba v ETS.
Je tiež pozoruhodné, že medziprodukty cyklu TCA sa môžu použiť aj ako prekurzory rôznych biosyntetických procesov.
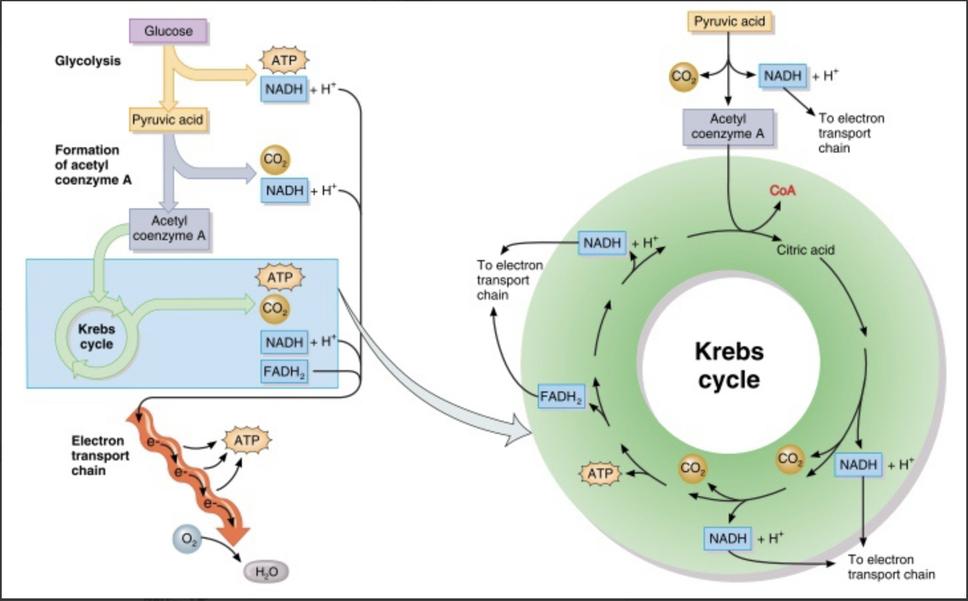
Cyklus TCA je známy aj ako Krebsov cyklus, pomenovaný po svojom objaviteľovi Sirovi Hansovi Krebsovi.

Krebs založil svoju koncepciu tohto cyklu na štyroch hlavných pozorovaniach uskutočnených v 30. rokoch 20. storočia.
Prvým bol objav v roku 1935 postupnosti reakcií od sukcinátu cez fumarát po malát po oxalacetát Albertom Szent-Gyorgyim, ktorý ukázal, že tieto dikarboxylové kyseliny prítomné v živočíšnych tkanivách stimulujú spotrebu O2.

Druhým bolo nájdenie sekvencie od citrátu cez α-ketoglutarát až po sukcinát v roku 1937 Carlom Martiusom a Franzom Knoopom.
Ďalej to bolo pozorovanie samotného Krebsa, ktorý pracoval na kultúrach svalových plátkov, že pridanie trikarboxylových kyselín aj vo veľmi nízkych koncentráciách podporuje oxidáciu oveľa vyššieho množstva pyruvátu, čo naznačuje katalytický účinok týchto zlúčenín. A štvrtým bolo Krebsovo pozorovanie, že malonát, inhibítor sukcinátdehydrogenázy, úplne zastavil oxidáciu pyruvátu pridaním trikarboxylových kyselín a že pridanie oxalacetátu do média v tomto stave vytváralo citrát, ktorý sa hromadil, čím elegantne ukázal cyklický charakter cesty.
Cesty degradácie živín, ktoré konvergujú do cyklu TCA
Glykolýza - je cesta, pri ktorej sa jedna molekula glukózy degraduje na dve molekuly pyruvátu.
Je zaujímavé, že počas počiatočnej fázy sa spotrebúva energia, pretože dve molekuly ATP sa využívajú na aktiváciu glukózy a fruktóza-6-fosfátu. Časť energie získanej rozpadom fosfoanhydridovej väzby ATP sa zachová pri tvorbe fosfát-esterových väzieb v glukózo-6-fosfáte a fruktóza-1,6-bifosfáte. V druhej časti glykolýzy sa väčšina voľnej energie získanej oxidáciou aldehydovej skupiny glyceraldehyd-3-fosfátu (G3P) zachová v acylfosfátovej skupine 1,3-bisfosfoglycerátu (1,3-BPG) , ktorý obsahuje vysokú voľnú energiu. Potom sa časť potenciálnej energie 1,3BPG, uvoľnenej počas jeho premeny na 3-fosfoglycerát, spojí s fosforyláciou ADP na ATP.
Druhou reakciou, pri ktorej dochádza k syntéze ATP, je premena fosfoenolpyruvátu (PEP) na pyruvát. PEP je vysokoenergetická zlúčenina vďaka svojej fosfát-esterovej väzbe, a preto je konverzná reakcia PEP na pyruvát spojená s fosforyláciou ADP. Tento mechanizmus syntézy ATP sa nazýva fosforylácia na úrovni substrátu.
Na úplnú oxidáciu sa molekuly pyruvátu generované v glykolýze transportujú do mitochondriálnej matrice, aby sa premenili na acetyl-CoA v reakcii katalyzovanej multienzýmovým komplexom pyruvátdehydrogenázy.
Keď Krebs v roku 1937 navrhol cyklus TCA, myslel si, že citrát bol syntetizovaný z oxaloacetátu a pyruvátu (alebo ich derivátu). Ale až po Lipmannovom objave koenzýmu A v roku 1945 a následnej práci R. Sterna, S. Ochoa a F. Lynena sa ukázalo, že molekula acetyl-CoA darovala svoju acetylovú skupinu oxalacetátu. Dovtedy bol TCA cyklus vnímaný iba ako cesta k oxidácii sacharidov. A práve väčšina hlavne stredoškolských učebníc odráža toto obdobie vedomostí o biochémii a nezdôrazňuje, ako sa cesty degradácie lipidov a aminokyselín zbiehajú v cykle TCA.
Oxidačná dráha mastných kyselín pretína cyklus TCA

V roku 1904 Knoop v klasickom experimente rozhodne ukázal, že oxidácia mastných kyselín je proces, pri ktorom sa dvojuhlíkové jednotky postupne odstraňovali z molekuly karboxylovej mastnej kyseliny.
Proces pozostáva zo štyroch reakcií a generuje acetyl-CoA a molekulu acyl-CoA skrátenú o dva uhlíky, so súčasnou redukciou FAD enzýmom acyl-CoA dehydrogenázou a NAD+ β-hydroxyacyl-CoA dehydrogenázou.
Táto cesta je známa ako β-oxidácia, pretože β-uhlíkový atóm sa oxiduje skôr, ako sa štiepi väzba medzi uhlíkmi β a α. Štyri kroky β-oxidácie sa kontinuálne opakujú, kým sa acyl-CoA úplne nezoxiduje na acetyl-CoA, ktorý potom vstúpi do cyklu TCA.
V 50. rokoch 20. storočia séria experimentov overila, že atómy uhlíka mastných kyselín sú rovnaké, aké sa objavili v kyselinách cyklu TCA.
Transaminácia/deaminácia aminokyselín Prispieva k cyklu TCA
Pokiaľ ide o použitie aminokyselín ako paliva v energetickom metabolizme, je potrebné vnímať dve veci.
Prvou je prítomnosť dusíka v zložení aminokyselín, ktorý sa musí odstrániť skôr, ako sa aminokyseliny stanú metabolicky užitočnými. Druhou je, že existuje najmenej dvadsať rôznych aminokyselín, z ktorých každá vyžaduje inú degradačnú dráhu.
Pre nás je dôležité spomenúť dva druhy reakcií zahŕňajúcich aminokyseliny: transamináciu a deamináciu.
V prvom druhu reakcie enzýmy aminotransferázy konvertujú aminokyseliny na ich príslušné a-ketokyseliny prenesením aminoskupiny jednej aminokyseliny na a-ketokyselinu. Táto reakcia umožňuje vzájomnú premenu aminokyselín. Druhý typ reakcie, deaminácia, odstraňuje aminoskupinu aminokyseliny vo forme amoniaku.
V pečeni má zase oxidačná deaminácia glutamátu za následok α-keto-glutarát (medziprodukt cyklu TCA) a amoniak, ktorý sa premieňa na močovinu a vylučuje sa. Deaminačné reakcie v iných orgánoch tvoria amoniak, ktorý je vo všeobecnosti začlenený do glutamátu za vzniku glutamínu, ktorý je hlavným transportérom aminoskupín v krvi. Všetky aminokyseliny sa teda prostredníctvom transaminačných/deaminačných reakcií môžu premeniť na medziprodukty cyklu TCA, priamo alebo prostredníctvom konverzie na pyruvát alebo acetyl-CoA.
Zhrnutie
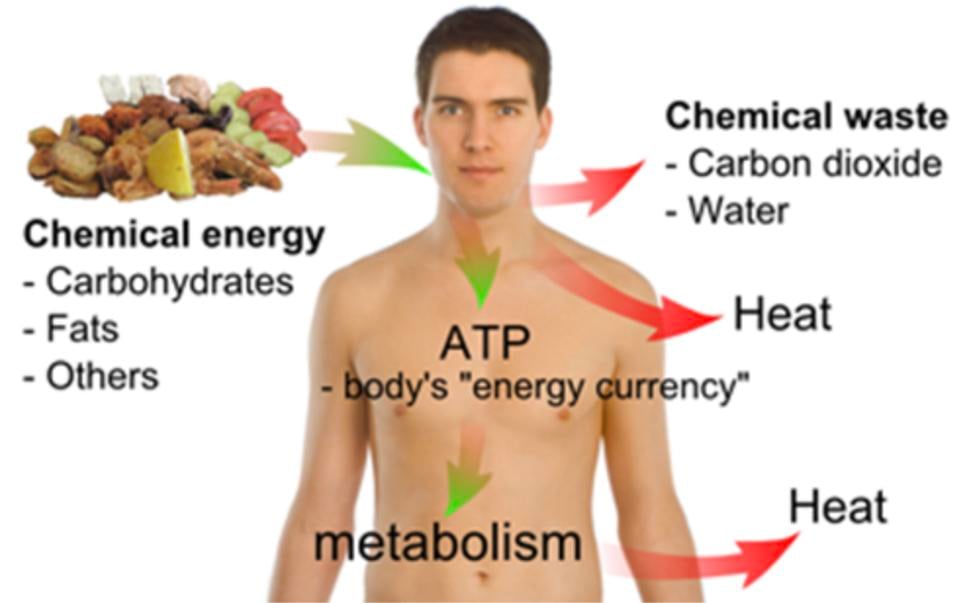
Transformácia chemickej energie molekúl paliva na užitočnú energiu je v našom ľudskom tele prísne regulovaná a využitie glukózy, mastných kyselín a aminokyselín rôznymi bunkami riadi niekoľko faktorov.
Napríklad nie všetky bunky majú enzýmový mechanizmus a správne bunkové odseky na využitie všetkých troch tipov molekúl paliva.
Napríklad červené krvinky vôbec neobsahujú mitochondrie, a preto nie sú schopné oxidovať ani mastné kyseliny, ani aminokyseliny, pri syntéze ATP sa spoliehajú iba na glukózu.
Navyše, dokonca aj v bunkách, ktoré môžu využívať všetky živiny, sa typ potravinového substrátu, ktorý sa oxiduje, mení podľa fyziologickej situácie bunky, ako je stav sýtosti a hladovania.
Existujú rôzne „signály“, ktoré určujú, ako sa bunky môžu prispôsobiť každej situácii, ako sú hormóny, ktoré môžu mať silné účinky prepnutím kľúčových enzýmových aktivít v priebehu niekoľkých sekúnd, alebo ako môžu modulovať profil génovej expresie, čím sa mení metabolický profil celej bunky. Preto je nutné komplexne chápať všetky metabolické dráhy ako integrované deje kontrolujúce reguláciu a premenu energie.
Skrátka naše telo je zázrak a záhada, ktoré stále lúštime...





